In diesem Video gehen wir auf eine interessante Studie aus Taiwan ein. Die Studie untersucht mögliche Zusammenhänge zwischen der Schumann-Resonanz und Schlaflosigkeit.

Schlafstörungen gehören zu den häufigsten Gesundheitsproblemen unserer Zeit. Eine aktuelle Studie von Fachleuten untersucht den Zusammenhang zwischen der natürlichen Schumann-Resonanz – elektromagnetischen Schwingungen der Erde – und Schlaflosigkeit. Die Ergebnisse geben spannende Hinweise auf mögliche Einflüsse natürlicher Frequenzen auf den menschlichen Schlaf.
Yu-Shu Huang (1,2), I Tang (1), Wei-Chih Chin (1,2), Ling-Sheng Jang (3), Chin-Pang Lee (1,2), Chen Lin (4), Chun-Pai Yang (5,6), Shu-Ling Cho (7)
(1) 1Abteilung für Kinder- und Jugendpsychiatrie und Schlafzentrum, Chang Gung Memorial Hospital, Taoyuan, Taiwan;
(2) Medizinische Fakultät der Chang Gung Universität, Taoyuan, Taiwan;
(3) Fachbereich Elektrotechnik, Nationale Cheng-Kung-Universität, Tainan, Taiwan;
(4) Fachbereich Biomedizinische Wissenschaften und Technik, Nationale Zentraluniversität, Taoyuan, Taiwan;
(5) Abteilung für Neurologie, Kuang Tien Allgemeines Krankenhaus, Taichung, Taiwan;
(6) Fachbereich Ernährung, Huang-Kuang-Universität, Taichung, Taiwan;
(7) Fachbereich Klinische Psychologie, Fu Jen Catholic University, New Taipei City, Taiwan;
Zahlreiche Studien haben gezeigt, dass elektromagnetische Felder das menschliche Gehirn und den Schlaf beeinflussen können und dass
extrem niederfrequente elektromagnetische Felder, sogenannte Schumann-Resonanzen, möglicherweise zur Linderung von Schlafstörungen beitragen
können. Ziel dieser Studie war es, die Reaktionen von Patienten mit Schlafstörungen auf eine nicht-invasive Behandlung mit Schumann-Resonanzen
(SR) zu untersuchen und deren Wirksamkeit anhand subjektiver und objektiver Schlafbewertungen zu beurteilen.
Wir haben ein doppelblindes und randomisiertes Design verwendet, und 40 Teilnehmer (70 % weiblich; 50,00 ± 13,38
Jahre) mit Schlafstörungen haben die gesamte Studie abgeschlossen. Diese Teilnehmer wurden in die SR-Schlafgerät-Gruppe und die Placebo-Gerät
Gruppe aufgeteilt und vier Wochen lang beobachtet. Die Studie verwendete Polysomnographie (PSG) zur Messung des objektiven Schlafes und verwendete Schlaftagebücher, den Pittsburgh Sleep Quality Inventory (PSQI), die Epworth Sleepiness Scale (ESS) und eine visuelle Analogie der
Schlafzufriedenheit zur Messung des subjektiven Schlafes. Der 36-Item Short-Form Health Survey (SF-36) wurde zur Bewertung der Lebensqualität verwendet. Zur Analyse der Daten wurden der Chi-Quadrat-Test, der Mann-Whitney-U-Test und der Wilcoxon-Test verwendet.
Etwa 70 % der Probanden waren Frauen mit einem Durchschnittsalter von 50 ± 13,38 Jahren und einer durchschnittlichen Schlafstörungen-Vorgeschichte von 9,68 ± 8,86 Jahren. Wir stellten fest, dass in der SR-Schlafgerät-Gruppe die objektiven Schlafmessungen (Einschlafzeit, SOL, und Gesamtschlafzeit, TST) und die subjektiven Schlaf-Fragebögen (SOL, TST, Schlafeffizienz, Schlafqualität, Tagesmüdigkeit und Schlafzufriedenheit) nach der Verwendung des SR-Schlafgeräts signifikant verbessert waren; In der Placebo-Geräte-Gruppe wurden nur subjektive Schlafverbesserungen wie PSQI und Schlafzufriedenheit beobachtet.
Diese Studie zeigt, dass das SR-Schlafgerät die Symptome von Schlaflosigkeit sowohl durch objektive als auch subjektive Tests mit minimalen Nebenwirkungen reduzieren kann. Zukünftige Studien können den möglichen Mechanismus von SR und die Auswirkungen auf die Gesundheit untersuchen und mit einer längeren Nachbeobachtungszeit die Wirksamkeit und Nebenwirkungen überprüfen.vinar dapibus leo.
Schlaflosigkeit, Schumann-Resonanz, Wirksamkeit, Polysomnographie, Fragebogen
Schlaflosigkeit ist die weltweit häufigste Schlafstörung und betrifft bis zu 10 % der Gesamtbevölkerung und etwa 15 % der Erwachsenen (1). Gemäß der Internationalen Klassifikation der Schlafstörungen, dritte Ausgabe (ICSD-3), wird Schlaflosigkeit definiert als
(1) Schwierigkeiten beim Einschlafen, Durchschlafen oder Aufwachen vor der gewünschten Zeit;
(2) Schlafstörungen, die zu erheblichen persönlichen Belastungen oder Beeinträchtigungen des täglichen Lebens führen; und
(3) Schlafstörungen und damit verbundene Tagesbeschwerden, die mindestens dreimal pro Woche über einen Zeitraum von mindestens drei Monaten auftreten.
Schlaflosigkeit umfasst nicht nur Schlafstörungen in der Nacht, sondern auch eine Beeinträchtigung der Tagesfunktionen wie Müdigkeit, Aufmerksamkeits- und Gedächtnisstörungen, Beeinträchtigungen der sozialen, schulischen oder beruflichen Leistungsfähigkeit sowie Stimmungsschwankungen.
Darüber hinaus haben viele Studien gezeigt, dass Menschen mit Insomnie ein höheres Risiko für Herz-Kreislauf-Erkrankungen, chronische Schmerzen und Typ-II-Diabetes haben.
Darüber hinaus liegt die Komorbiditätsrate von Insomnie und anderen psychischen Störungen bei 41–53 %.
Nach einer kognitiven Verhaltenstherapie bei Schlaflosigkeit (CBTi) haben Patienten mit komorbiden psychischen Erkrankungen nicht nur verbesserte Symptome der Schlaflosigkeit, sondern auch verbesserte Symptome der Komorbiditäten.
Obwohl die pathophysiologischen Merkmale der Schlaflosigkeit weitgehend unbekannt sind, gibt es zunehmend Hinweise darauf, dass Schlaflosigkeit ein anhaltender Zustand und eine komplexe Erkrankung ist. Eine Kohortenstudie mit 3073 Erwachsenen, die über einen Zeitraum von 5 Jahren jährlich nachuntersucht wurden, bestätigte, dass 41,6 % der Teilnehmer an einer anhaltenden Insomnie litten. Dieser Befund legt nahe, dass eine frühzeitige Intervention die Entwicklung einer chronischen Insomnie verhindern und die damit verbundene Morbidität durch Sedativa und Schlafmittel reduzieren könnte.
Frühere Studien haben gezeigt, dass bis zu 13 % der Erwachsenen in den USA angaben, im letzten Jahr Benzodiazepine eingenommen zu haben. Auch die ambulante Verwendung von Benzodiazepinen hat deutlich zugenommen. Die langfristige Einnahme und Überdosierung von Schlafmitteln kann zu Nebenwirkungen führen.
Obwohl die Leitlinien zur Behandlung von Schlaflosigkeit etablierte Empfehlungen für die klinische Praxis zur CBTi als Erstbehandlung enthalten, hat sich diese Behandlungsmethode in vielen Ländern bisher nicht durchgesetzt. Darüber hinaus sind die Unannehmlichkeiten und die Compliance der Patienten mit CBTi nach wie vor zentrale Probleme bei der Umsetzung dieser Behandlung. Daher ist es wichtig, die Wirksamkeit anderer und neuerer nicht-pharmazeutischer Behandlungsmethoden für Schlaflosigkeit zu untersuchen.
In den letzten Jahren wurden verschiedene nicht-invasive Behandlungsmethoden für Schlaflosigkeit erforscht, darunter Achtsamkeitstherapie, Akupressur, Akupunkturtherapien, kraniale Elektrotherapie-Stimulation (CES) oder repetitive transkranielle Magnetstimulation (rTMS) usw. Eine weitere besondere Entdeckung der letzten 20 Jahre ist, dass elektromagnetische Schwankungen in der Umgebung, wie z. B. geomagnetische Aktivitäten, unsere Physiologie, Psychologie und unser Verhalten beeinflussen können. Frühere physikalische Forschungen zeigten, dass „eine elektroenzephalographische Leistung bestimmte Zusammenhänge mit dem rechten Parietallappen für Theta-Aktivität und der rechten Frontalregion für Gamma-Aktivität aufwies”. und einige Studien haben moderate Korrelationen zwischen einer Zunahme der geomagnetischen Aktivität und verschiedenen Verhaltensfolgerungen der Gehirnaktivität gezeigt.
Wang et al. (2019) verwendeten eine Elektroenzephalogramm-Studie (EEG) und berichteten über eine starke, spezifische Reaktion des menschlichen Gehirns auf ökologisch relevante Rotationen der Magnetfelder der Erde. Nach geomagnetischer Stimulation kam es wiederholt zu einem Abfall der Amplitude der EEG-Alpha-Oszillationen (8–13 Hz).
Im Jahr 1954 berichtete Winfried Otto Schumann über die Existenz eines natürlichen extrem niederfrequenten Feldes von etwa 7,83 Hz, der sogenannten Schumann-Resonanzfrequenz (SR) in der Erdatmosphäre, die elektromagnetische Wellen (EMW) global ausbreitet. 27 Ihre Spitzenintensität kann bei ~8 Hz nachgewiesen werden, zusammen mit ihren Oberschwingungen mit einer geringeren Intensität bei 14, 20, 26, 33, 39 und 45 Hz aufgrund frequenzbedingter ionosphärischer Ausbreitungsverluste.
Die Schumann-Resonanzen, die sowohl in der globalen quantitativen elektroenzephalographischen Aktivität des Menschen als auch in der Aktivität der Erdionosphäre gefunden wurden, könnten auf einen kausalen Zusammenhang hindeuten.
Darüber hinaus fanden Ghione et al. signifikante positive Zusammenhänge zwischen der geomagnetischen Aktivität und dem systolischen Blutdruck (tagsüber und über 24 Stunden) sowie dem diastolischen Blutdruck (tagsüber, nachts und über 24 Stunden). Burch et al. fanden außerdem heraus, dass eine zunehmende geomagnetische Aktivität in Verbindung mit erhöhten 60-Hz-MF mit einer verringerten nächtlichen Ausscheidung eines Melatonin-Metaboliten beim Menschen einhergeht, was bedeutet, dass EMF das menschliche Gehirn und den Schlaf beeinflussen.
Angesichts dieser gesammelten Erkenntnisse könnte extrem niederfrequente EMF-Schumann-Resonanz den menschlichen Schlaf verbessern. In dieser Studie verwenden wir ein Schlafgerät mit „Schumann-Resonanz”-Funktion, das die niedrige Frequenz der „Schumann-Resonanzfrequenz (7,83 Hz)-Welle” ausgibt, um die Gehirnwellen des Benutzers in Resonanz zu versetzen und so das Einschlafen, das Erreichen des Tiefschlafs und die Aufrechterhaltung des Schlafs zu erleichtern. Da die Wirksamkeit und Nebenwirkungen der „Schumann-Wellen” bei der Behandlung von Schlaflosigkeit noch unklar sind, zielte diese Studie darauf ab, die Auswirkungen der Schumann-Resonanz auf Schlaflosigkeitssymptome durch subjektive und objektive Schlafbewertungen zu untersuchen.
In dieser Studie wurden Patienten mit Schlaflosigkeit über ambulante Kliniken von Krankenhäusern rekrutiert, und 46 Teilnehmer erfüllten die Einschlusskriterien und nahmen nach Abgabe ihrer Einverständniserklärung an der Studie teil. Von diesen schieden vier aus, da sie nicht zum Nachuntersuchungstermin erscheinen konnten, und zwei Teilnehmer litten nach der Randomisierung unter Kopfschmerzen und Schwindel und brachen die Nachuntersuchung ab. Insgesamt schlossen 40 Teilnehmer die Studie ab. Die Studie wurde von Chang 1114 Powered by TCPDF (www.tcpdf.org) https://doi.org/10.2147/NSS.S346941 Nature and Science of Sleep 2022:14 Powered by TCPDF (www.tcpdf.org) DovePress Dovepress Huang et al Gung Hospital IRB: Nr. 201701063A3 und Nr. 202101267B0 (klinische Studien-ID: NCT05053919, Studienzeitraum: 27.7.2021 bis 19.1.2022) und entsprach der Deklaration von Helsinki.
Die Einschlusskriterien umfassen (1) Teilnehmer im Alter zwischen 20 und 70 Jahren; (2) Teilnehmer müssen die DSM-5-Diagnosekriterien für Schlaflosigkeit erfüllen und seit mehr als drei Monaten diagnostiziert sein; (3) Teilnehmer müssen bereit sein, eine Einverständniserklärung zu unterzeichnen; und (4) Teilnehmer, die Schlafmittel einnehmen, müssen sich verpflichten, während der Studie keine Änderungen an der Medikation und Dosierung vorzunehmen.
Zu den Ausschlusskriterien gehören (1) Teilnehmer, die Herzschrittmacher oder Herzmonitore verwenden; (2) Teilnehmer mit schweren körperlichen Erkrankungen oder nach Operationen, wie Herzerkrankungen, Stoffwechselerkrankungen oder Krebs; (3) Teilnehmer mit schweren psychischen Störungen, wie Schizophrenie, schwerer Major Depression, schwerer Angststörung, bipolarer Störung, Demenz, Substanzmissbrauch; oder schweren neurologischen Erkrankungen, wie Krampfanfällen, Schlaganfall oder Parkinson; (4) Teilnehmer mit anderen schweren Schlafstörungen, wie schwerer obstruktiver Schlafapnoe, schwerem periodischem Bewegungsdrang oder Narkolepsie; (5) Teilnehmer, die nicht in der Lage sind, regelmäßig an Nachuntersuchungen teilzunehmen; und (6) Teilnehmer, die keine gute Schlafhygiene einhalten können und nicht in der Lage sind, vor dem Schlafengehen auf die Nutzung elektronischer Geräte zu verzichten.
Bei dieser Studie handelt es sich um eine randomisierte Doppelblind-Fallkontrollstudie. Alle Teilnehmer, die die Einschlusskriterien erfüllten, wurden nach dem Zufallsprinzip der „SR-Schlafgerät-Gruppe” oder der „Placebo-Gerät-Gruppe” zugewiesen. Es gab keine signifikanten Unterschiede zwischen den beiden Gruppen hinsichtlich der Hintergrundvariablen wie Geschlechterverhältnis, Alter und Dauer der Schlaflosigkeit.
Alle Teilnehmer wurden nach dem Zufallsprinzip zwei Gruppen zugeordnet und verwendeten das „Schlafgerät“ vier Wochen lang.
Der primäre Endpunkt sind die Veränderungen in der Polysomnographie, und die sekundären Endpunkte sind Veränderungen in den subjektiven Fragebögen, darunter der Pittsburgh Sleep Quality Inventory (PSQI) und die Epworth Sleepiness Scale (ESS), die Schlaftagebücher, die visuelle Analogskala zur Schlafzufriedenheit und der 36-Item Short-Form Health Survey (SF-36).
Das SR-Gerät wurde von Professor Ling-Sheng Zhang von der National Cheng Kung University in Taiwan entwickelt (Abbildung 1: „Enerkey Kingdom SR Sleep Device“). Das Schlafgerät war in der Lage, die „niederfrequente Schumann-Resonanzfrequenz (7,83 Hz) Welle” zu erzeugen und erhielt am 4. Mai 2016 das taiwanesische Patent (Nr. TW M530656U). Nach dem Einschalten des Schlafgeräts gibt es stabil die zusammengesetzte Frequenz aus „Schumann-Resonanzfrequenz (7,83 Hz) Welle, Theta-Welle und Delta-Welle” aus. Ein Placebo-Gerät ist ein Gerät, das genauso aussieht und funktioniert wie das SR-Schlafgerät, jedoch keine Frequenzwellen ausgibt. Die Probanden wurden gebeten, das Gerät vier Wochen lang jede Nacht zu verwenden (es neben dem Bett in Richtung des Kopfes des Probanden zu platzieren, es jeden Abend etwa eine Stunde vor dem Schlafengehen einzuschalten und es am nächsten Tag nach dem Aufstehen auszuschalten) und ihren Schlaf in Schlafprotokollen aufzuzeichnen.
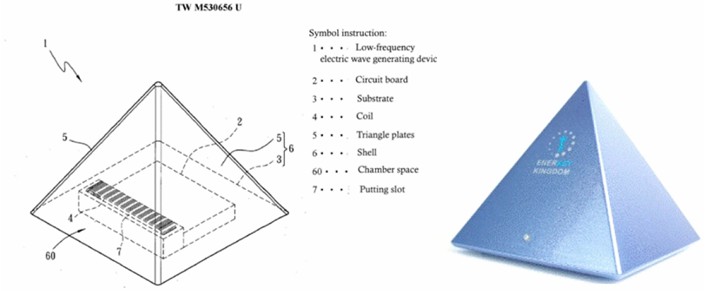
Eine standardmäßige nächtliche PSG wurde durchgeführt, um den Schlaf aller Teilnehmer vor der Verwendung des SR-Schlafgeräts/Placebo-Geräts und vier Wochen nach der Verwendung zu dokumentieren. Die Teilnehmer wurden gebeten, um 21 Uhr zu erscheinen, wurden von einem Schlaftechniker in den Untersuchungsraum geführt, wo sie ein Sensorgerät angelegt bekamen, und legten sich um 22 Uhr auf das Bett. Die Untersuchung endete am nächsten Morgen gegen 6 Uhr. Die standardmäßige nächtliche polysomnographische Untersuchung umfasste die systematische Überwachung der folgenden Variablen: 4 EEG-Ableitungen, 2 Elektrookulogramm-Ableitungen (EOG), Kinn- und Bein-Elektromyogramm-Ableitungen (EMG) und 1 Elektrokardiogramm-Ableitung (EKG); Die Atmung wurde mit einem Nasenkanülen-Druckwandler, einem Mundthermistor, induktiven Plethysmographie-Bändern für Brustkorb und Bauch, einem Fingersauerstoffsättigungsmessgerät (MasimoTM) mit Ableitung von Oximetrie- und Fingerplethysmographiesignalen, einem Halsmikrofon, diaphragmatisch-interkostalen und abdominalen Muskel-EMGs sowie einer transkutanen CO2-Elektrode überwacht; außerdem wurden die Bein-EMGs überwacht. Die Probanden wurden während der Aufzeichnung kontinuierlich per Video überwacht. Die Aufzeichnungen wurden gemäß den Empfehlungen der American Academy of Sleep Medicine (AASM) durchgeführt, und die PSG-Auswertung erfolgte ebenfalls gemäß den AASM-Empfehlungen, wobei Hypopnoe entweder bei einem Abfall der Sauerstoffsättigung um 3 % oder bei einer Erregungsreaktion bewertet wurde.
Die Teilnehmer füllten die Schlaftagebücher zwei Wochen lang täglich aus, bevor sie das SR-Schlafgerät/Placebo-Gerät verwendeten, und vier Wochen lang während der Verwendung des Geräts, um ihren Schlaf aufzuzeichnen. Aus den Tagebüchern wurde eine Schätzung für den Durchschnitt von SOL, TST, SE und WASO berechnet.
Der PSQI ist ein Fragebogen zur Selbsteinschätzung der subjektiven Schlafqualität, der aus 19 Fragen besteht und zu 7 klinisch abgeleiteten Komponentenscores (0–3) berechnet und kombiniert werden kann, wobei höhere Werte eine schlechtere Schlafqualität anzeigen.33,34 Die Teilnehmer füllten den PSQI vor der Verwendung, zwei Wochen nach der Verwendung und vier Wochen nach der Verwendung des SR-Schlafgeräts/Placebo-Geräts aus.
Der ESS besteht aus 8 Punkten (jeweils mit einer Punktzahl von 0 bis 3) und wurde verwendet, um die Tagesmüdigkeit der einzelnen Personen zu bewerten. 35 Teilnehmer füllten den ESS vor der Verwendung, zwei Wochen nach der Verwendung und vier Wochen nach der Verwendung des SR-Schlafgeräts/Placebo-Geräts aus.
Die Probanden wurden außerdem gebeten, vor der Anwendung und vier Wochen nach der Anwendung anhand einer Sieben-Punkte-Skala ihre Zufriedenheit mit ihrem Schlaf in der vergangenen Woche zu bewerten (eine höhere Punktzahl steht für eine höhere Zufriedenheit mit dem Schlaf).
SF-36 umfasst 11 wichtige Fragen, die acht Komponenten bewerten. Zu diesen Komponenten gehören körperliche Funktionsfähigkeit, Einschränkungen aufgrund körperlicher Gesundheit, Einschränkungen aufgrund emotionaler Probleme, Energie/Müdigkeit, emotionales Wohlbefinden, soziale Funktionsfähigkeit, Schmerzen und allgemeiner Gesundheitszustand. Die Skala kann verwendet werden, um die allgemeine Lebensqualität eines Patienten einzuschätzen. Höhere Werte bedeuten eine bessere körperliche oder geistige Funktionsfähigkeit.
Wir haben unsere Daten mit SPSS 22.0 analysiert. Die Daten wurden als Anzahl, Mittelwert, Prozentsatz und Standardabweichung dargestellt. Wir haben den Chi-Quadrat-Test für Gruppenvergleiche des Prozentsatzes und den Mann-Whitney-U-Test verwendet, um die Unterschiede in den objektiven und subjektiven Messungen zwischen der SR-Schlafgerätgruppe und der Placebogruppe zu analysieren. Wir haben den Wilcoxon-Test verwendet, um die Unterschiede vor und nach der Verwendung des Geräts zu analysieren. Ein p-Wert von weniger als 0,05 wurde als signifikant angesehen.
Etwa 70 % der 40 Probanden waren Frauen mit einem Durchschnittsalter von 50 ± 13,38 Jahren und einer durchschnittlichen Schlafstörungen-Vorgeschichte von 9,68 ± 8,86 Jahren. Tabelle 1 listet die Merkmale der Teilnehmer zu Beginn der Studie auf. Es wurden keine signifikanten Unterschiede hinsichtlich Geschlecht, Alter, Dauer der Schlafstörungen, Bildungsstand, Familienstand, sozioökonomischem Status oder Komorbidität zwischen den beiden Gruppen festgestellt.
Vergleiche der objektiven Schlafmessungen vor und vier Wochen nach der Verwendung des SR-Schlafgeräts/Placebo-Geräts sind in Tabelle 2 dargestellt. In der SR-Schlafgerät-Gruppe wurde eine signifikante Verringerung der SOL (p = 0,012) und eine signifikante Erhöhung der TST (p = 0,037) beobachtet. In der Placebo-Geräte-Gruppe wurde kein signifikanter Unterschied beobachtet. Obwohl es vor und nach der Behandlung keinen signifikanten Unterschied zwischen den beiden Gruppen gab (Mann-Whitney-U-Test), gab es einen Trend, dass sich viele Parameter der SR-Schlafgerät-Gruppe verbesserten, insbesondere die SOL (p = 0,055).
Tabelle 1: Demografische Daten der SR-Sleep-Gerätegruppe und der Placebo-Gerätegruppe
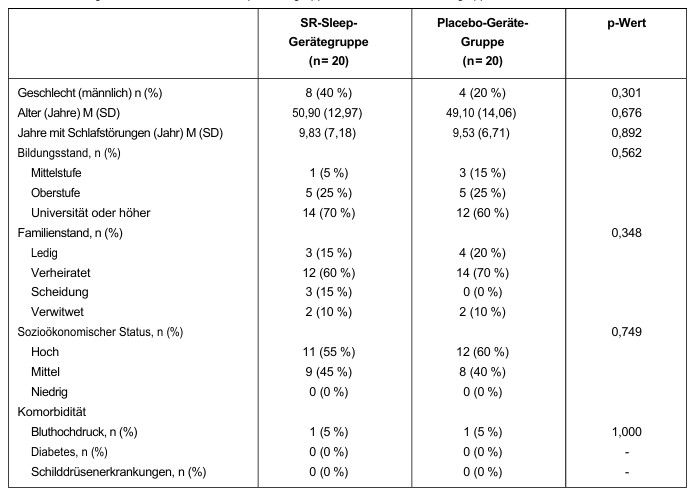
Tabelle 2: Unterschiede der objektiven PSG-Befunde in der SR-Sleep-Geräte-/Placebo-Geräte-Gruppe
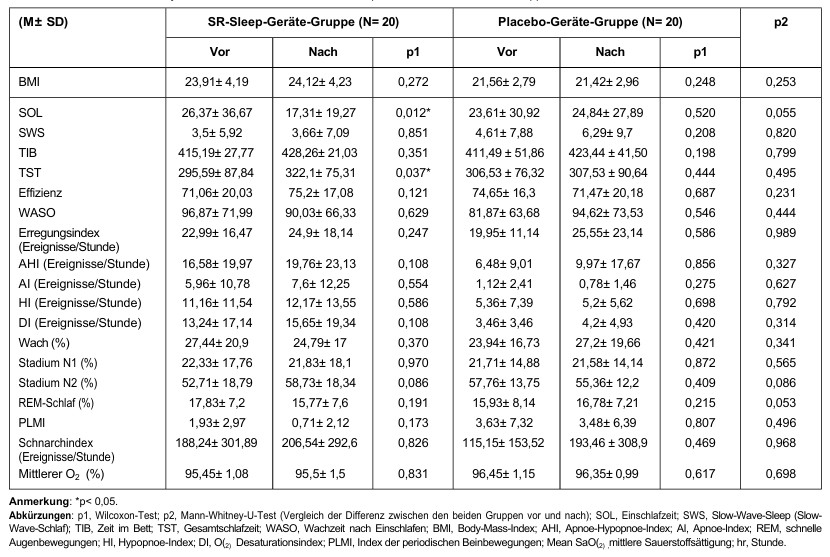
Vergleiche der subjektiven Schlafmessungen vor, zwei Wochen nach und vier Wochen nach der Verwendung des SR-Schlafgeräts/Placebo-Geräts sind in Tabelle 3 dargestellt.
In der SR-Schlafgerät-Gruppe wurde eine signifikante Verringerung der SOL (p = 0,004) und eine signifikante Erhöhung der TST (p = 0,047) und SE (p = 0,017) beobachtet (alle Unterschiede bestanden zwischen der Voruntersuchung und Woche 4). In der Placebo-Gerät-Gruppe wurde kein signifikanter Unterschied beobachtet.
Eine signifikante Verringerung des Schlaflatenzindex (p = 0,003, die Signifikanz lag zwischen „vorher, Woche 2” und „Woche 4”) wurde in der SR-Schlafgerät-Gruppe beobachtet, nicht jedoch in der Placebo-Gerät-Gruppe. Signifikante Verbesserungen des subjektiven Schlafqualitätsindex (pSR = 0,001 (vorher > Woche 2, Woche 4); pplacebo = 0,042 (vor der Behandlung > Woche 2)), des Schlafdauerindex (pSR = 0,021 (vor der Behandlung > Woche 2); pplacebo = 0,009 (vor der Behandlung > Woche 2, Woche 4)), des Gesamtindex (pSR = 0,034 (vor der Behandlung > Woche 2, Woche 4); pplacebo = 0,044 (vor > Woche 2, Woche 4)) und ESS (pSR = 0,019 (vor > Woche 4, p = 0,055)) wurden in beiden Gruppen beobachtet. Darüber hinaus verbesserte sich der Parameter „Schlafqualität” der SR-Schlafgerät-Gruppe signifikant (p = 0,046).
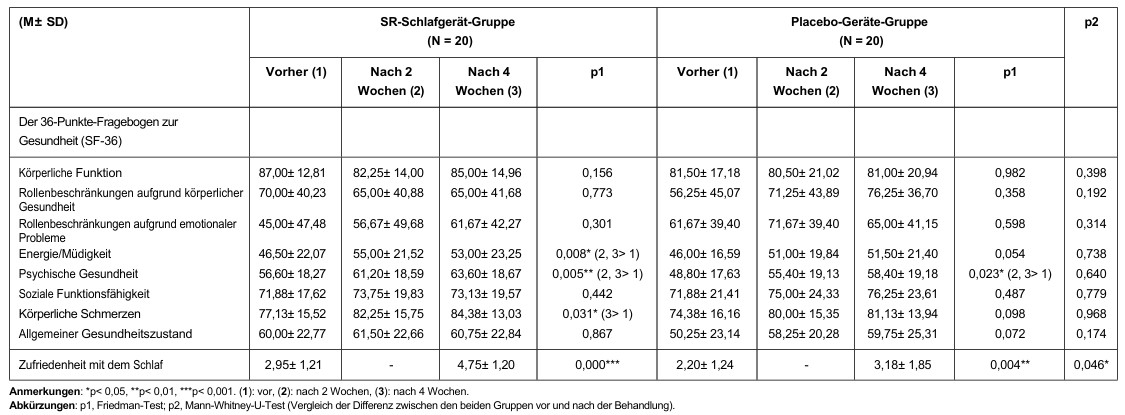
Vergleiche der subjektiven Lebensqualität (SF-36) vor, 2 Wochen nach und 4 Wochen nach der Verwendung des SR-Schlafgeräts/Placebo-Geräts sind in Tabelle 4 dargestellt. Signifikante Verbesserungen in Bezug auf Energie/Müdigkeit (p = 0,008) und körperliche Schmerzen (p = 0,031) wurden in der SR-Schlafgerät-Gruppe beobachtet, nicht jedoch in der Placebo-Gerät-Gruppe. Wir beobachteten signifikante Verbesserungen der psychischen Gesundheit (pSR = 0,005; pPlacebo = 0,023) in beiden Gruppen. Die Schlafzufriedenheit verbesserte sich in beiden Gruppen signifikant (pSR < 0,001; pPlacebo = 0,004). Darüber hinaus war die Veränderung des Schlafzufriedenheitswerts gegenüber dem Ausgangswert (p = 0,046) in der SR-Schlafgerät-Gruppe größer als in der Placebo-Gerät-Gruppe.
Tabelle 3: Unterschiede der subjektiven Schlafmessungen in der SR-Sleep-Geräte-/Placebo-Geräte-Gruppe
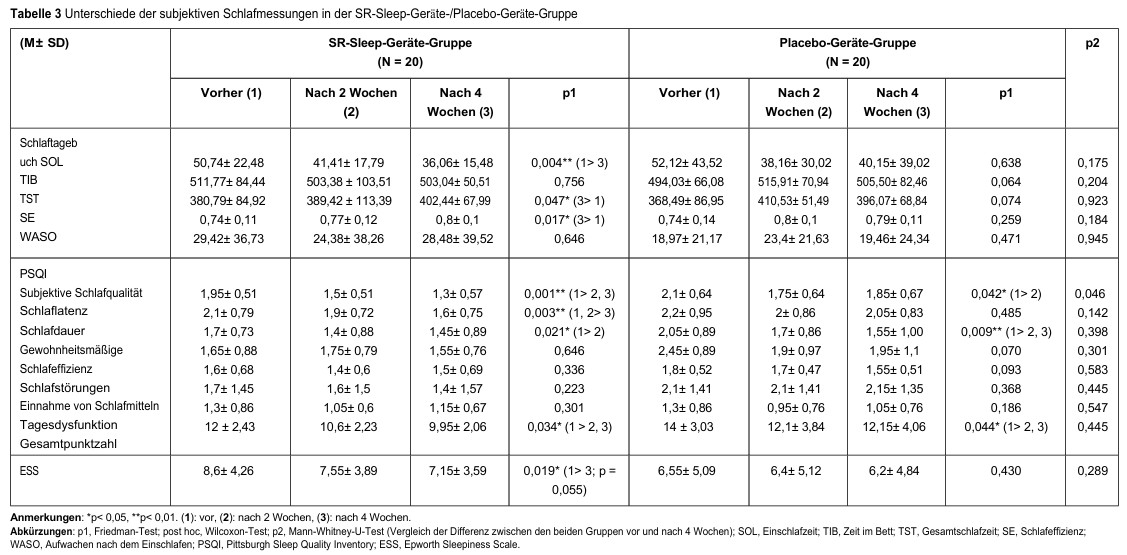
Tabelle 4: Unterschiede zwischen der Gesundheitsumfrage (SF-36) und der Schlafzufriedenheit in der SR-Sleep-Geräte-/Placebo-Geräte-Gruppe
Von den 46 Teilnehmern litten zwei Teilnehmer unter Kopfschmerzen und Schwindel bei der Verwendung des Geräts (1 gehörte zur SR-Schlafgerätgruppe und 1 zur Placebo-Gerätgruppe) und brachen die Teilnahme ab. Es gab keine weiteren unerwünschten Ereignisse.
Diese Studie untersucht, ob 40 Teilnehmer mit Schlafstörungen nach vierwöchiger Anwendung eines SR-Schlafgeräts/Placebo-Geräts Verbesserungen bei subjektiven und objektiven Schlafmessungen erzielen können. Nur zwei Teilnehmer litten unter Nebenwirkungen wie Kopfschmerzen und Schwindel (Studiengruppe n = 1; Placebogruppe n = 1) und brachen die Studie ab. Diese Studie ist die erste, die untersucht, ob SR den Schlaf und Schlafstörungen beeinflusst.
In der SR-Schlafgerät-Gruppe verbesserten sich sowohl die objektiven PSG-Messungen (SOL und TST, jedoch nicht SWS) als auch die subjektiven Schlafmessungen (SOL, TST, SE, Schlafqualität, Tagesmüdigkeit, Schlafzufriedenheit) nach der Verwendung des SR-Schlafgeräts signifikant. In der Placebo-Geräte-Gruppe zeigten die objektiven Schlafmessungen jedoch keine Unterschiede nach der Verwendung des Geräts, und es gab nur eine subjektive Verbesserung des Schlafes in Bezug auf die Schlafzufriedenheit und einige Komponenten des PSQI.
Dieses Ergebnis deutet darauf hin, dass SR die Symptome von Schlaflosigkeit reduzieren kann, insbesondere in Bezug auf das „Einschlafen” und die „Gesamtschlafzeit”. Eine weitere wichtige Erkenntnis ist, dass 55 % der Placebo-Gruppe eine Verbesserung gemäß PSQI und Schlafzufriedenheitsskala zeigten, was durch den üblichen Placebo-Effekt bei der Behandlung von Schlaflosigkeit erklärt werden kann.
Derzeit verstehen wir den Mechanismus des SR bei der Verbesserung von Schlaflosigkeit und Schlaf noch nicht vollständig. Frühere Studien haben gezeigt, dass Veränderungen der geomagnetischen Aktivität mit epileptischen Anfällen, Myokardinfarkt, Schlaganfall und Depressionen in Verbindung gebracht werden. Biogenes Magnetit bietet einen molekularen Mechanismus für die geomagnetische Wahrnehmung, der im menschlichen Gehirn gefunden wurde.
Cherry (2002) vermuteten, dass SR, das extrem niederfrequente (ELF) Wellen global ausbreitet, „der mögliche biologische Mechanismus” ist, der die biologischen und gesundheitlichen Auswirkungen der geomagnetischen Aktivität auf den Menschen erklärt. Die Spitzenfrequenzen von SR unterliegen einer moderaten täglichen Schwankung von etwa ± 0,5 Hz. Interessanterweise liegen die ersten vier SR-Modi zufällig innerhalb des Frequenzbereichs der ersten vier EEG-Bänder (d. h. Delta 0,5–3,5 Hz, Theta 4–7 Hz, Alpha 8–13 Hz und Beta 14 bis 30 Hz).
Einige Studien haben auch festgestellt, dass menschliche Gehirnwellen und SR denselben Frequenzbereich haben. Der menschliche Körper erkennt, absorbiert und reagiert auf natürliche EMF durch den Prozess der Frequenzresonanzanpassung. Durch diese Anpassung können natürliche EMF biologische Kommunikationsphänomene in der Zell-zu-Zell-Kommunikation im menschlichen Körper beeinflussen.44 Pall (2013) berichtete auch, dass die Exposition gegenüber EMF den Ca2+-Einstrom über den spannungsgesteuerten Ca2+-Kanal fördern würde, was die Ca2+-Konzentration im Zytosol erhöhen und dann biologische Effekte verursachen kann.45 Wang (2019) wies ebenfalls darauf hin, dass extrem niederfrequente magnetische Stimulation niederfrequente Aktivitäten induzieren und zu Resonanzeffekten im menschlichen Gehirn führen kann.
Der „biophysikalische Mechanismus” für den Wirkungsmechanismus auf die menschliche Gesundheit könnte die biologischen und gesundheitlichen Auswirkungen der geomagnetischen Aktivität erklären. Immer mehr Psychiater integrieren elektrophysiotherapeutische Behandlungen in ihre klinische Praxis, da diese nicht invasiv sind, wenige Nebenwirkungen haben und gleichzeitig Angstzustände, Depressionen und Schlaflosigkeit behandeln können. Aus unseren Ergebnissen zur Verbesserung der SOL lässt sich ableiten, dass SR die Gehirnwellen der Teilnehmer mit 7,83-Hz-Wellen in Resonanz versetzen und ihren Körper entspannen kann, sodass sie leichter einschlafen und ihre Gesamtschlafzeit verlängern können. Eine weitere Hypothese ist, dass EMF mit menschlichen Melatonin-Metaboliten in Zusammenhang stehen, was ebenfalls die Verbesserung der Gesamtschlafzeit und Schlafqualität der Teilnehmer nach vierwöchiger Behandlung erklären könnte. Diese Studie zeigte jedoch keinen signifikanten Anstieg des Tiefschlafanteils (SWS %). Dies könnte mit der geringen Stichprobengröße oder dem First-Night-Effekt der PSG zusammenhängen. Die vierwöchige Behandlungsdauer ist möglicherweise zu kurz oder hat noch keinen Einfluss auf Melatonin. Daher erfordern diese Ergebnisse und Hypothesen strengere und langfristige Untersuchungen. Eine kürzlich durchgeführte systematische Überprüfung und Metaanalyse von CBTi zeigte signifikante Auswirkungen auf Tagesbeschwerden, einschließlich Tagesmüdigkeit, obwohl die Effektstärke nur gering bis mäßig ist. Durch die Verbesserung der nächtlichen Symptome kann CBTi einen positiven indirekten Effekt auf die Tagesbeschwerden haben. In ähnlicher Weise hat die SR-Schlafgerät-Gruppe in dieser Studie einen signifikanten Effekt auf das Ausmaß der Tagesmüdigkeit, was bedeutet, dass die SR die Lebensqualität von Insomniepatienten während des Tages (z. B. Energie/Müdigkeit, körperliche Schmerzen und psychische Gesundheit) verbessern kann. Darüber hinaus berichtete Kay, dass SR Depressionen verbessert.
Neben den möglichen Vorteilen für den Schlaf, die diese Studie gezeigt hat, müssen weitere therapeutische Wirkungen von SR, wie z. B. eine verbesserte Tagesmüdigkeit und Depressionen, sowie die Rolle von SR bei diesen korrelierten Zuständen weiter untersucht werden. Obwohl es sich um ein randomisiertes, doppelblindes Design handelt, gibt es dennoch Einschränkungen. Erstens war die Stichprobengröße sehr klein (N = 40), obwohl wir die geschätzte Stichprobengröße (N = 38) erreicht haben. Zweitens hatten mehrere Patienten Hypnotika erhalten und konnten diese nicht absetzen, aber sie behielten während der Studie die gleichen Medikamente und die gleiche Dosis bei. Es kann zu Stichprobenfehlern kommen, wenn wir nur Teilnehmer ohne Medikamenteneinnahme einbeziehen. Drittens sollte der „First-Night-Effekt” bei der Durchführung der PSG berücksichtigt werden, da er möglicherweise die Verbesserung in der PSG erklären kann. Allerdings zeigte nur die SR-Schlafgerät-Gruppe eine signifikante Verbesserung in der PSG, und dieser Befund stützte die Wirkung von SR auf den Schlaf. Darüber hinaus können wir die Compliance nicht wirklich überprüfen, aber wir haben unsere Teilnehmer während des Studienzeitraums darauf hingewiesen, das Gerät jede Nacht einzuschalten.
Diese Studie zeigt, dass die SR die Symptome von Schlaflosigkeit reduzieren kann, was sowohl durch objektive als auch subjektive Messungen bestätigt wird, obwohl die Stichprobengröße klein ist. Zukünftige Studien sollten die möglichen psychischen und physischen Auswirkungen der Schumann-Resonanz mit größeren Stichprobengrößen untersuchen sowie eine längere Nachbeobachtungszeit verwenden, um die Wirksamkeit und Nebenwirkungen zu überprüfen und mögliche Mechanismen zu erforschen.
Die Daten, die die Ergebnisse dieser Studie stützen, sind nach Erhalt der Genehmigung der Ethikkommission des Chang Gung Hospital auf begründete Anfrage beim Erstautor oder korrespondierenden Autor erhältlich. Darüber hinaus sind die anonymisierten Daten der einzelnen Teilnehmer nach Kontaktaufnahme mit dem Erstautor oder korrespondierenden Autor per E-Mail erhältlich. Die Daten sind unmittelbar nach der Veröffentlichung ohne Enddatum verfügbar.
Diese Studie wurde von Professor Guilleminault vor seinem Tod am 9. Juli 2019 konzipiert. Obwohl er nicht als korrespondierender Autor dieser Studie fungieren konnte, möchten wir ihm unseren Dank und unsere Anerkennung aussprechen. Er gehörte zu den wichtigsten und grundlegendsten Persönlichkeiten auf dem Gebiet der Schlafmedizin. Ohne seine Inspiration und Vision hätten wir diese Studie nicht abschließen können. Diese Studie wurde durch die Förderungen Nr. CMRPG 3J 0131 und 3J 0133 des Chang Gung Memorial Hospital an Dr. Yu-Shu Huang und die Förderung Nr. CMRPG 3L0291 des Chang Gung Memorial Hospital an Dr. Wei-Chih Chin unterstützt.
Die Autoren erklären, dass sie keine finanziellen Vereinbarungen oder Verbindungen im Zusammenhang mit dieser Studie haben. Diese Forschung erhielt keine spezifischen Zuschüsse von Förderinstitutionen aus dem öffentlichen, kommerziellen oder gemeinnützigen Sektor. Das Patent TW M530656 U (SR-Gerät) gehört Professor Ling-Sheng Jang. Die Autoren geben keine weiteren Interessenkonflikte in dieser Arbeit an.
1. Morin CM, Benca R. Chronische Schlaflosigkeit. Lancet. 2012;379:1129–1141. doi:10.1016/S0140-6736(11)60750-2
2. Amerikanische Akademie für Schlafmedizin. Die internationale Klassifikation der Schlafstörungen.
3. Auflage. Darien (IL): Amerikanische Akademie für Schlafmedizin; 2014. 3. Bertisch SM, Pollock BD, Mittleman MA et al. Schlaflosigkeit mit objektiv kurzer Schlafdauer und Risiko für Herz-Kreislauf-Erkrankungen und Gesamtmortalität: Schlaf-Herz-Gesundheitsstudie. Sleep. 2018;41:zsy047. doi:10.1093/sleep/zsy047
4. Generaal E, Vogelzangs N, Penninx BW, et al. Schlaflosigkeit, Schlafdauer, depressive Symptome und das Auftreten chronischer muskuloskelettaler Schmerzen an mehreren Stellen. Sleep. 2017;40:zsw030.
5. Hein M, Lanquart JP, Loas G, et al. Prävalenz und Risikofaktoren von Typ-2-Diabetes bei Menschen mit Insomnie: eine Studie mit 1311 Personen, die zu Schlafuntersuchungen überwiesen wurden. Sleep. 2018;46:37–45. doi:10.1016/j.sleep.2018.02.006
6. Harvey AG. Schlaflosigkeit: Symptom oder Diagnose? Clin Psychol Rev. 2001;21:1037–1059. doi:10.1016/S0272-7358(00)00083-0 1122 Powered by TCPDF (www.tcpdf.org) https://doi.org/10.2147/NSS.S346941 Natur und Wissenschaft des Schlafs 2022:14 Powered by TCPDF (www.tcpdf.org) DovePress Dovepress Huang et al
7. Baglioni C, Battagliese G, Feige B, et al. Schlaflosigkeit als Prädiktor für Depressionen: eine metaanalytische Auswertung longitudinaler epidemiologischer Studien. J Affect Disord. 2011;135:10–19. doi:10.1016/j.jad.2011.01.011
8. Dolsen MR, Asarnow LD, Harvey AG. Schlaflosigkeit als transdiagnostischer Prozess bei psychiatrischen Störungen. Curr Psychiatry Rep. 2014;16:471. doi:10.1007/s11920-014-0471-y
9. Sateia MJ, Buysse DJ, Krystal AD et al. Klinische Praxisleitlinie für die pharmakologische Behandlung von chronischer Schlaflosigkeit bei Erwachsenen: eine klinische Praxisleitlinie der American Academy of Sleep Medicine. J Clin Sleep Med. 2017;13:307–349. doi:10.5664/jcsm.6470
10. Morin CM, Jarrin DC, Ivers H et al. Inzidenz, Persistenz und Remissionsraten von Insomnie über einen Zeitraum von 5 Jahren. JAMA Netw Open. 2020;3:e2018782. doi:10.1001/jamanetworkopen.2020.18782
11. Maust DT, Lin LA, Blow FC. Benzodiazepin-Konsum und -Missbrauch bei Erwachsenen in den Vereinigten Staaten. Psychiatr Serv. 2019;70:97–106. doi:10.1176/ appi.ps.201800321
12. Agarwal SD, Landon BE. Muster bei der Verschreibung von Benzodiazepinen in der ambulanten Versorgung in den Vereinigten Staaten. JAMA Netw Open. 2019;2:e187399. doi:10.1001/ jamanetworkopen.2018.7399
13. Buscemi N, Vandermeer B, Friesen C, et al. Die Wirksamkeit und Sicherheit von medikamentösen Behandlungen bei chronischer Schlaflosigkeit bei Erwachsenen: eine Metaanalyse von RCTs. J Gen Intern Med. 2007;22:1335–1350. doi:10.1007/s11606-007-0251-z
14. Glass J, Lanctôt KL, Herrmann N, et al. Sedativa und Hypnotika bei älteren Menschen mit Insomnie: Metaanalyse der Risiken und Vorteile. BMJ. 2005;331:1169. doi:10.1136/bmj.38623.768588.47
15. Edinger JD, Arnedt JT, Bertisch SM, et al. Verhaltens- und psychologische Behandlungen für chronische Insomnie bei Erwachsenen: eine klinische Praxisrichtlinie der American Academy of Sleep Medicine. J Clin Sleep Med. 2021;17:255–262. doi:10.5664/jcsm.8986
16. Ong J, Sholtes D. Ein achtsamkeitsbasierter Ansatz zur Behandlung von Schlaflosigkeit. J Clin Psychol. 2010;66:1175–1184. doi:10.1002/jclp.20736
17. Gong H, Ni CX, Liu YZ, et al. Achtsamkeitsmeditation bei Schlaflosigkeit: eine Metaanalyse randomisierter kontrollierter Studien. J Psychosom Re. 2016;89:1–6. doi:10.1016/j.jpsychores.2016.07.016
18. Carotenuto M, Gallai B, Parisi L, et al. Akupressurtherapie bei Schlaflosigkeit bei Jugendlichen: eine polysomnographische Studie. Neuropsychiatr Dis Treat. 2013;9:157. doi:10.2147/NDT.S41892
19. Yeung WF, Chung KF, Poon MMK, et al. Akupressur, Reflexzonenmassage und Ohrakupunktur bei Schlaflosigkeit: eine systematische Übersicht randomisierter kontrollierter Studien. Sleep Med. 2012;13:971–984. doi:10.1016/j.sleep.2012.06.003
20. Sok SR, Erlen JA, Kim KB. Auswirkungen der Akupunkturtherapie auf Schlaflosigkeit. J Adv Nurs. 2003;44:375–384. doi:10.1046/j.0309-2402.2003.02816.x
21. Yin X, Gou M, Xu J, et al. Wirksamkeit und Sicherheit der Akupunkturbehandlung bei primärer Insomnie: eine randomisierte kontrollierte Studie. Sleep Med. 2017;37:193–200. doi:10.1016/j.sleep.2017.02.012
22. Kirsch DL, Nichols F. Elektrotherapie-Stimulation des Schädels zur Behandlung von Angstzuständen, Depressionen und Schlaflosigkeit. Psychiatr Clin North Am. 2013;36:169–176. doi:10.1016/j.psc.2013.01.006
23. He Y, Sun N, Wang Z, Zou W. Wirkung der repetitiven transkraniellen Magnetstimulation (rTMS) bei Schlaflosigkeit: ein Protokoll für eine systematische Überprüfung. BMJ open. 2019;9:e029206. doi:10.1136/bmjopen-2019-029206
24. Belisheva NK, Popov AN, Petukhova NV, et al. Qualitative und quantitative Bewertung der Auswirkungen von Schwankungen des Erdmagnetfelds auf die Funktionsfähigkeit des menschlichen Gehirns. Biofizika. 1995;40:1005–1012.
25. Mulligan BP, Suess-Cloes L, Mach QH, et al. Geopsychologie Geophysikalische Matrix und menschliches Verhalten. Der Mensch und die Geosphäre, Nova Science Publishers; 2010:115–141.
26. Wang CX, Hilburn IA, Wu DA, et al. Transduktion des Erdmagnetfeldes, nachgewiesen durch Alpha-Band-Aktivität im menschlichen Gehirn. eneuro. 2019;6(2):ENEURO.0483–18.2019. doi:10.1523/ENEURO.0483-18.2019
27. Sentman DD. Schumann-Resonanzen. In: Volland H, Herausgeber. Handbuch der atmosphärischen Elektrodynamik. Boca Raton (FL): CRC Press; 1995:267–298.
28. Cherry N. Schumann-Resonanzen, ein plausibler biophysikalischer Mechanismus für die Auswirkungen der Sonne auf die menschliche Gesundheit. Naturgefahren. 2002;26:279–331. doi:10.1023/A:1015637127504
29. Persinger MA. Schumann-Resonanzfrequenzen in quantitativer elektroenzephalographischer Aktivität: Auswirkungen auf die Wechselwirkungen zwischen Erde und Gehirn. Int Lett Chem Phys Astron. 2014;11:24–32. doi:10.18052/www.scipress.com/ILCPA.30.24
30. Ghione S, Mezzasalma L, Del Seppia C, et al. Beeinflussen geomagnetische Störungen solarer Herkunft den arteriellen Blutdruck? J Hum Hypertens. 1998;12:749–754. doi:10.1038/sj.jhh.1000708
31. Burch JB, Reif JS, Yost MG. Geomagnetische Störungen stehen im Zusammenhang mit einer verminderten nächtlichen Ausscheidung eines Melatonin-Metaboliten beim Menschen. Neurosci Lett. 1999;266:209–212. doi:10.1016/S0304-3940(99)00308-0
32. Rechtschaffen A, Kales A. Ein Handbuch mit standardisierten Begriffen, Techniken und Bewertungssystemen für die Schlafphasen von Menschen. Psychiatry Clin Neurosci. 1968;55:305–310.
33. Buysse DJ, Reynolds CF, Monk TH et al. Der Pittsburgh-Schlafqualitätsindex: ein neues Instrument für die psychiatrische Praxis und Forschung. Psychiatrieforschung. 1989;28:193–213. doi:10.1016/0165-1781(89)90047-4
34. Tsai PS, Wang SY, Wang MY, et al. Psychometrische Bewertung der chinesischen Version des Pittsburgh-Schlafqualitätsindex (CPSQI) bei primärer Insomnie und Kontrollpersonen. Qual Life Res. 2005;14(8):1943–1952.
35. Johns MW. Eine neue Methode zur Messung der Tagesmüdigkeit: die Epworth-Schläfrigkeitsskala. Sleep. 1991;14:540–545. doi:10.1093/sleep/14.6.540
36. Brazier JE, Harper R, Jones NM, et al. Validierung des SF-36-Fragebogens zur Gesundheitsbefragung: neues Ergebnismaß für die Primärversorgung. BMJ. 1992;305:160–164. doi:10.1136/bmj.305.6846.160
37. Koffel EA, Koffel JB, Gehrman PR. Eine Metaanalyse der kognitiven Verhaltenstherapie in Gruppen bei Schlaflosigkeit. Sleep Med Rev. 2015;19:6–16. doi:10.1016/j.smrv.2014.05.001
38. Persinger MA, Psych C. Plötzlicher unerwarteter Tod bei Epileptikern nach plötzlichen, intensiven Erhöhungen der geomagnetischen Aktivität: Prävalenz des Effekts und mögliche Mechanismen. Int J Biometeorol. 1995;38:180–187. doi:10.1007/BF01245386
39. Stoupel E, Abramson E, Sulkes J, et al. Zusammenhang zwischen Suizid und Myokardinfarkt im Hinblick auf sich verändernde physikalische Umweltbedingungen. Int J Biometeorol. 1995;38:199–203. doi:10.1007/BF01245389
40. Feigin VL, Nikitin YP, Vinogradova TE. Sonnen- und geomagnetische Aktivitäten: Gibt es einen Zusammenhang mit dem Auftreten von Schlaganfällen? Cerebrovasc Dis. 1997;7:345–348. doi:10.1159/000108220
Um Ihnen ein optimales Erlebnis zu bieten, verwenden wir Technologien wie Cookies, um Geräteinformationen zu speichern und/oder darauf zuzugreifen. Wenn Sie diesen Technologien zustimmen, können wir Daten wie das Surfverhalten oder eindeutige IDs auf dieser Website verarbeiten. Wenn Sie Ihre Einwilligung nicht erteilen oder zurückziehen, können bestimmte Merkmale und Funktionen beeinträchtigt werden.